通常情况下,海水是酸性还是碱性?A.碱性B.酸性正确答案:A答案解析:通常情况下,海水是碱性的,而不是酸性。
海水的pH值通常介于7.5至8.4之间,稍微偏向碱性。
这是由于海水中存在一定量的碳酸盐和碱性物质,例如氢氧化钠(NaOH)和碳酸钙(CaCO3),它们导致海水呈现碱性。
海水中有着丰富的各种资源,出了能晒盐之外,我们还可以从中提取出碱,这也是我们日常生活和生产中经常用到的重要物质。
所以海洋资源是需要我们尽全力进行维护的,它是我们各种资源的来源。
第三节 海水“制碱”
一、氨碱法制纯碱
精制 吸氨 碳酸化 过滤、热解
(1) (2)
(1)NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl
(2)2 NaHCO3
Na2CO3+ CO2↑+H2O
1、碳酸钠:俗称:纯碱或苏打,
用途:
2、碳酸氢钠:俗称:小苏打 ( 用途一定得看噢 )
用途:
二、纯碱的性质
1、纯碱的化学性质
(1)、与指示剂的的作用
纯碱能使无色酚酞变红,证明溶液呈碱性。
(2)、与酸的反应
Na2CO3+2HCl=2NaCl+H2O+CO2↑(用于检验碳酸根离子)
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
实例:检验一瓶无色溶液中含有碳酸根离子
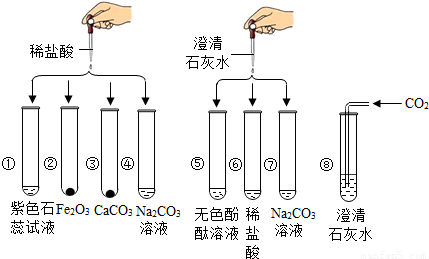
取无色溶液少许注入试管,向试管中加入稀盐酸,将产生的气体通入澄清石灰水,如果石灰水变浑浊,证明产生二氧化碳,因此证明原溶液中含有碳酸根。
(3)、与氢氧化钙的反应
Ca(OH)2+ Na2CO3= CaCO3↓+2NaOH 工业制氢氧化钠
(4)、与氯化钡的反应
Na2CO3+BaCl2=2NaCl+BaCO3↓
2、盐的溶解性
钾、钠、硝酸、铵盐溶
盐酸盐中银不溶(氯化银不溶于水)
碳酸盐溶钾、钠、铵
硫酸盐中钡不溶(硫酸钡不溶于水)
碱中钾、钠、钡、钙溶
3、盐的性质
(1)、与指示剂的的作用
纯碱能使无色酚酞变红,证明溶液呈碱性
(2)、盐+金属——另一种盐+另一种金属
①化学方程式
Fe+ CuSO4= FeSO4+Cu现象:铁的表面覆盖一层红色物质,溶液由蓝色变为浅绿色
Cu+2 AgNO3=2Ag+ Cu(NO3)2
②金属活动性顺序表的应用
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
a、只有排在前面的金属才能把排在后面的金属置换出来
b、这里的盐必须为盐溶液
c、K Ca Na除外

③波尔多液为什么不能用铁桶来盛(波尔多液的成分为氢氧化钙和硫酸铜)
Fe+ CuSO4= FeSO4+Cu

(3)、盐+酸——另一种酸+另一种盐
①化学方程式
2HCl+Na2CO3=2NaCl+H2O+CO2↑用于检验碳酸根离子
HCl+AgNO3=AgCl↓+HNO3用于检验氯离子
H2SO4+BaCl2=BaSO4↓+2HCl用于检验硫酸根离子
②实例:检验一瓶无色溶液中含有氯离子(硫酸根离子)
取无色溶液少许注入试管,向试管中加入硝酸银(氯化钡),然后滴入稀硝酸,如果产生的沉淀不溶解,证明原溶液中含有氯离子(硫酸根离子)。
(4)、盐+碱——另一种碱+另一种盐
盐和碱要反应:反应物必须溶于水,生成物必须有沉淀、气体、水生成
Ca(OH)2+ Na2CO3= CaCO3↓+2NaOH 工业制氢氧化钠
Ca(OH)2+CuSO4=Cu(OH)2↓+ CaSO4现象:产生蓝色沉淀
2NaOH+ CuSO4= Cu(OH)2↓+Na2 SO4现象:产生蓝色沉淀
3NaOH+ FeCl3=Fe(OH)3↓+3NaCl现象:产生红褐色沉淀

(5)、盐+盐——另外两种新盐
盐和盐要反应:反应物必须溶于水,生成物必须有沉淀、气体、水生成
Na2SO4+BaCl2= BaSO4↓+2NaCl
NaCl+ AgNO3= AgCl↓+NaNO3
复制本文链接攻略资讯文章为拓城游所有,未经允许不得转载。